合作客戶/
拜耳公司 |
同濟大學 |
聯合大學 |
美國保潔 |
美國強生 |
瑞士羅氏 |
相關新聞Info
-
> 植物油中N-酰基氨基酸表面活性劑的界面活性和聚集行為——材料和方法
> 生物膜是如何形成的?
> α-環糊精對非離子表面活性劑和兩性離子表面活性劑混合體系的界面及自組裝性質——結論
> 微尺度區域內靜電相互作用力動態調節和脂質雙分子層的分布——結果和討論
> 分子表面包裝對于磷脂單分子層膜中的錨定蛋白中酶活性的調制作用的影響——材料和方法
> 化纖油劑配制過程與表面張力之間的影響分析
> 極復雜問題背后的簡潔數學
> LB膜分析儀-α-短螺旋抗菌肽對癌細胞選擇性及其抗癌作用的分子機制:結果、討論、結論、致謝!
> 原油油品表面張力與納米級復合降凝劑的性質和溫度有何關系
> 從張力角度來解釋兩個小固體漂浮在液面上會靠近還是遠離
內分泌物在膠束中的增溶作用——結果和討論
來源:Kibron 瀏覽 1060 次 發布時間:2021-09-22
結果和討論
不同hp-β-CD濃度下NP溶液的界面張力
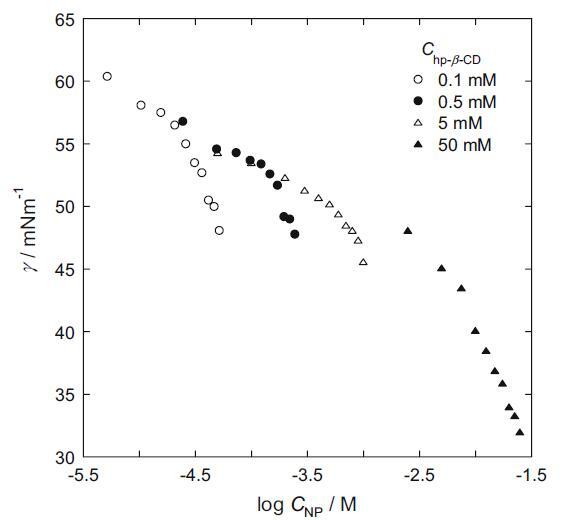
圖 1 不同 hp-β-CD 濃度下的界面張力 (γ) vs. log CNP/mol dm-3
NP 溶液在不同 hp-β-CD 濃度下的界面張力(γ)如圖 1 所示。在任何 hp-β-CD 濃度下,界面張力隨著 NP 的增加而降低。 Hp-β-CD 由七個葡萄糖單元組成,形成一個具有親水外表面和疏水內腔的環,眾所周知,它主要以 1:1 的化學計量將客體分子結合到疏水腔中 [11]。 在 hp-β-CD 的水溶液中,NP 被認為結合了 hp-β-CD 的疏水腔。 眾所周知,Hp-β-CD 由于其親水性外表面而不吸附在空氣-溶液界面。 這表明未摻入 hp-β-CD 腔的 NP 分子吸附在空氣 - 溶液界面。 在任何 hp-β-CD 濃度下均未觀察到表明膠束化開始的斷點(即臨界膠束濃度 (cmc))。 由于 NP 非常疏水,體相中的 NP 單體濃度不能增加到 cmc。 根據 γ 與 log CS,非離子 NP 的最大表面過量 (Γmax) 通過 Gibb 吸附方程估計如下 [12]:
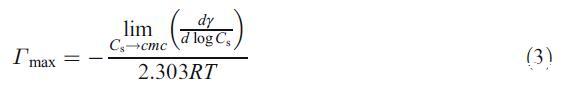
其中 CS 和 R 分別是 NP 濃度和氣體常數。 表面過量值列于表 1。表面過量值在任何 hp-β-CD 濃度下幾乎恒定,平均值為 4.6 μmol m-2。 這意味著 hp-β-CD 不影響吸附在空氣-溶液界面上的 NP 分子的取向。 與 HTAB 的表面過量值 (3.9 μmol m-2) [6] 相比,NP 在空氣-溶液界面處每個分子所占的面積似乎比 HTAB 小。 HTAB 的頭部基團與 HTAB 親水部分的三個甲基的體積之間的靜電排斥力抑制了擁擠的堆積。
表1 不同hp-β-CD濃度下NP的表面過量(Γmax)值

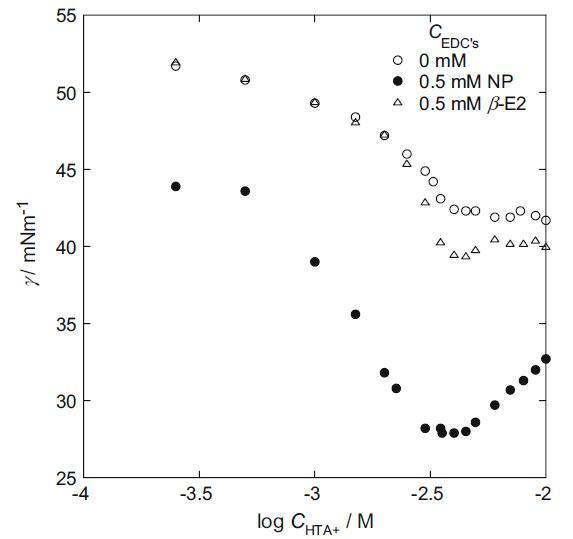
圖 2 存在各種內分泌干擾物時的界面張力 (γ) 與 log CHTA +/mol dm-3 的關系:5 mM hp-β-CD、0.49 M Na2SO4 和 0.01 M H2SO4
HTA+ 溶液與 hp-β-CD 和硫酸根離子的界面張力
為了研究支持電解質對空氣-溶液界面處 HTA+ 吸附性能的影響,我們測量了含有硫酸根離子的 HTA+ 溶液的界面張力。 含硫酸根離子的 HTA+ 溶液的界面張力如圖 2 所示。HTA+ 離子的 cmc 和最大表面過量值列于表 2。在大量支持電解質存在下 HTA+ 的表面過量值為由方程估計 (3) 其中 CS 是 HTA+ 濃度。 這些 cmc 值遠大于沒有 hp-β-CD 和硫酸根離子 (0.92 mM) [6] 時 HTAB 水溶液的 cmc 值。 這意味著 HTA+ 離子被并入 hp-β-CD 腔內,并且無 HTA+ 單體的濃度降低。 我們已經觀察到在兩種 EDC 存在下 HTA+ 的 cmc 值下降。 我們可以用兩個可能的原因來解釋 cmc 的這種下降。 第一個是 EDC 對膠束的穩定化。 這是由于羥基和 NP 或 β-E2 中芳香環的 C 電子與 HTA+ 離子中帶正電的銨部分之間的吸引力相互作用。 它降低了膠束中 HTA+ 極性頭基團之間的靜電斥力 [13]。 此外,NP 或 β-E2 與 HTAB 膠束之間的疏水相互作用穩定了膠束化 [14]。 第二個是兩個 EDC 分子都占據了 hp-β-CD 腔并增加了 HTA+-free 單體的濃度。 然而,NP de 比β-E2 更顯著地降低了cmc 值。 從分子結構來看,NP本身具有長碳鏈,類似于HTA+離子。 它使膠束形成中 HTA+ 和 NP 之間的親和力更高,并且更顯著地增加了不含 HTA+ 的單體的濃度。 盡管β-E2存在時HTAB的最大表面過剩值大于NP存在時的值,但后者EDC的界面張力遠低于前者。 在 NP 溶液中,NP 分子也被吸附在空氣-溶液界面,這也起到降低界面張力的作用。 然而,在 cmc 以上,隨著 CHTAB 和膠束濃度的增加,吸附的 NP 分子從空氣 - 溶液界面解吸并分布在膠束中,界面處 NP 的組成減少。 因此,界面張力再次大幅上升。
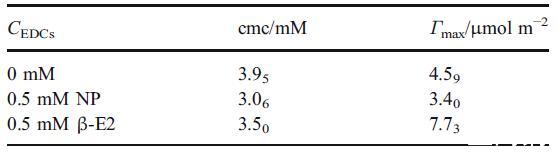
表 2 在含有 0.49 M Na2SO4 和 0.01 M H2SO4 的 5 mM hp-β-CD 存在下,HTA+ 溶液在不同 NP 或 β-E2 濃度下的 cmc 和表面過量 (Γmax) 值
熒光各向異性
RB 分子在膠束表面區域溶解得越硬,r 值越大[15]。 r 值的變化如圖 3 所示。在 0.1 mM 時,r 值下降。 這表明 EDCs 開始溶解到膠束中擾亂了 RB 分子在膠束表面的緊密堆積。 隨著NP濃度的增加,r值增加。 然而,隨著β-E2濃度的增加,r值一度恢復并似乎一點點下降。 這表明 NP 的增溶使膠束表面更加剛性,而 β-E2 的增溶則沒有。 NP在結構上更類似于HTA+。 因此,NP在膠束中的HTA+離子頭之間增溶,降低了膠束表面離子頭的靜電斥力,使膠束更加穩定和剛性[16]。 另一方面,β-E2 似乎會干擾 HTA+ 的取向并降低膠束表面的剛度。
DLS
我們在每個 EDC 存在下通過動態光散射方法研究了 HTA+ 膠束的 RH(圖 4)[17]。 隨著 EDCs 濃度的增加,膠束的流體動力學半徑似乎逐漸增加。
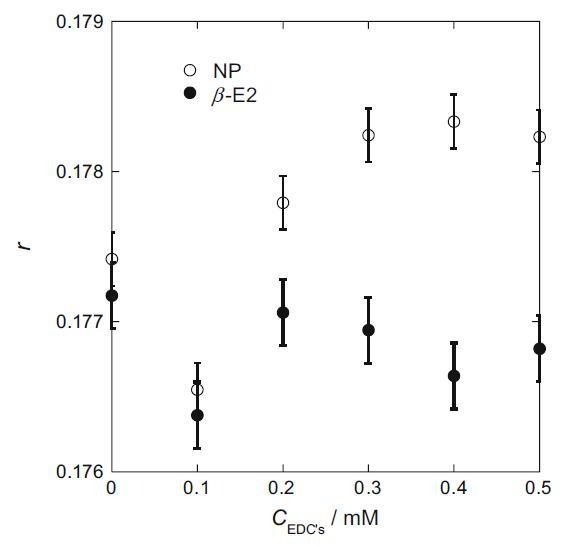
圖 3 熒光各向異性 (r) 值 vs. CEDCs/mM:50 mM hp-β-CD、20 mM HTAB、0.49 M Na2SO4 和 0.01 M H2SO4
這種趨勢在兩個 EDC 中是相似的。 在我們的芘熒光 I1/I3 實驗中,膠束中的極性不會因添加每個 EDC 而改變(數據未顯示)。 因此,流體動力學半徑的這種小幅增加不是由于膠束中水分子的侵入; 相反,這是由于EDC分子的入侵。 此外,EDCs 在膠束表面的侵入似乎降低了表面的電密度,并可能增加聚集數。
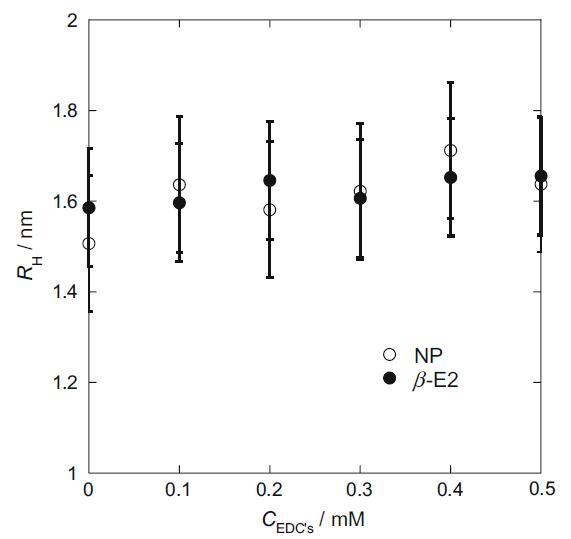
圖 4 膠束相對于 CEDCs/mM 的 RH:50 mM hp-β-CD、20 mM HTAB、0.49 M Na2SO4 和 0.01 M H2SO4
在 hp-β-CD 存在下 I2/I? 的循環伏安法
在這里,我們選擇 I2/I? 作為電化學探針,因為 I? 的電荷有望使其與陽離子膠束的結合變得容易,并且電中性 I2 有望在膠束中表面活性劑的疏水部分之間增溶并溶解在電極表面的表面活性劑單層中。 我們研究了 hp-β-CD 對 I2/I- 氧化還原峰的影響(圖 5)。 在沒有 hp-β-CD 的情況下,觀察到 I- 在約 530 mV 處的陽極峰和 I2 在約 480 mV 處的陰極峰。 在 50 mM hp-β-CD 存在下,陽極和陰極峰值電流均降低,并且它們的峰值電位向負方向移動。 陽極峰值電流的降低是由 I? 與 hp-β-CD 的親水表面結合引起的。 另一方面,陰極峰值電流的降低是由 hp-β-CD 疏水腔中包含 I2 引起的 [18]。 峰值電位的負移表明結合在 hp-β-CD 腔中的 I2 比結合到 hp-β-CD 表面的 I- 更穩定。
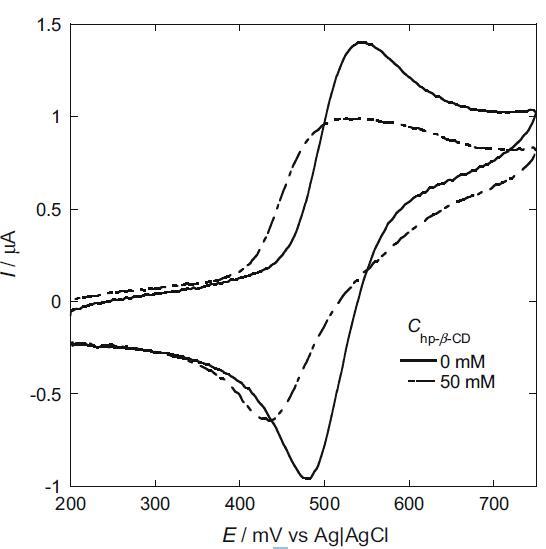
圖 5 存在 5 mM hp-β- 時 I2/I? 的循環伏安圖CD 和不存在 hp-β-CD:0.5 mM NaI、0.49 M Na2SO4、0.01 M H2SO4
在 HTA+ 離子和 hp-β-CD 存在下 I2/I? 的循環伏安法
我們還研究了 HTA+ 陽離子的影響(圖 6)。 來自界面張力測量的 HTA+ 離子的 cmc 與圖 6 標題中所述的 CV 測量溶液相同,為 3.95 mM。 I2/I? 的陽極和陰極峰均高于不存在 HTA+ 時的峰。 陽極和陰極峰值電流的增加是由于被捕獲的 I? 和 I2 從 hp-β-CD 釋放到主體中,這是由 hp-β-CD 腔中的 I? 和 I2 置換引起的與 HTA+。 另一方面,隨著 HTA+ 的濃度增加到 cmc 以上,陽極和陰極峰值電流都變得低于預膠束濃度下的峰值電流。 在 I2 和 I- 鍵合到膠束經歷電子轉移之前,膠束必須轉向,使 I2 和 I- 面向電極表面。 它導致峰值電流的降低。 此外,陽極和陰極峰值電位都向負方向移動。 這表明溶解在 HTA+ 膠束中的 I2 比鍵合到 HTA+ 膠束表面的 I- 更穩定。 隨著 HTA+ 濃度增加到 5 mM,在 330 mV 處觀察到一個尖銳的吸附減少峰。 已知在不存在任何表面活性劑的情況下,在鉑電極表面形成的 I2 會吸附在電極表面 [19]。 在我們的系統中,HTA+ 在低 HTA+ 濃度下抑制了 I2 的吸附。 然而,隨著HTA+濃度的增加,形成了HTA+單層,導致電極表面HTA+單層中的I2被吸收。 隨著 HTA+ 濃度增加至 10 mM,吸附還原峰消失。 在這個濃度下,在電極表面形成的 I2 溶解到 HTA+ 膠束中。 因此,沒有觀察到吸附峰。
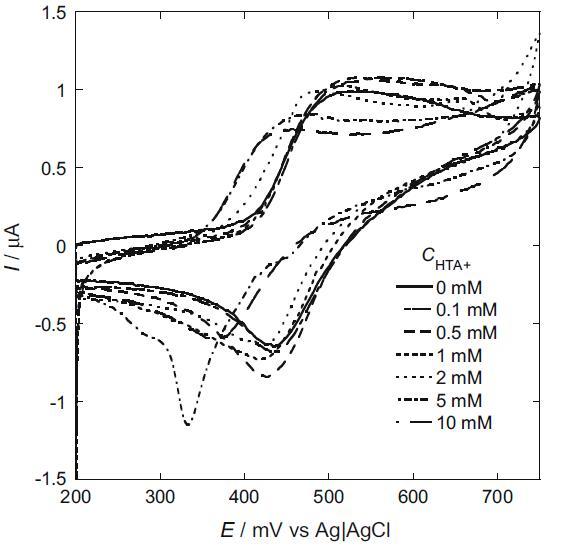
圖 6 不同 HTA+ 離子濃度下 I2/I? 的循環伏安圖:0.5 mM NaI、5 mM hp-β-CD、0.49 M Na2SO4、0.01 M H2SO4
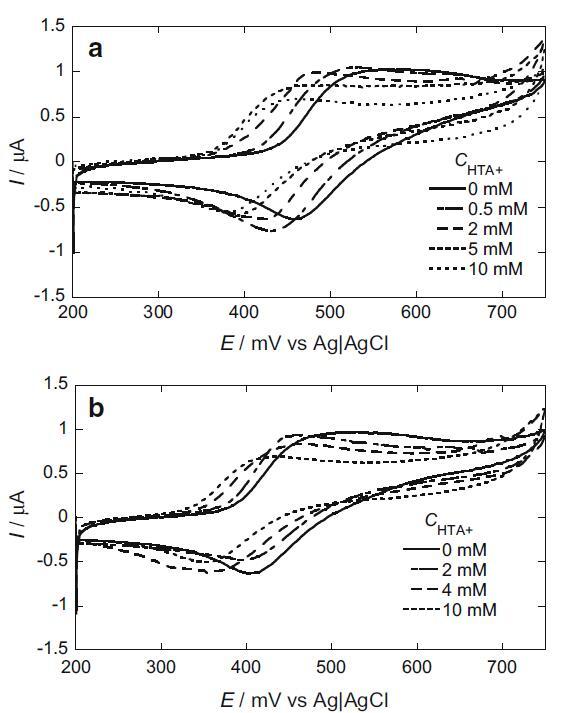
圖 7 在 0.5 mM NP (a) 或 0.5 mM β-E2 (b) 存在下,不同 HTA+ 離子濃度下 I2/I? 的循環伏安圖:0.5 mM NaI、5 mM hp-β-CD、0.49 M Na2SO4 , 0.01 M H2SO4
在 NP 或 β-E2、HTA+ 和 hp-β-CD 存在下 I2/I? 的循環伏安法
包含 NP 或 β-E2 的系統中 I2/I? 的循環伏安圖分別如圖 7a 和 b 所示。 根據界面張力測量結果,各個系統的 HTA+ 的 cmc 分別為 3.06 和 3.50 mM,并列于表 3 中。即使在 HTA+ 的預膠束濃度下,峰值電位也向負方向移動。 這表明即使在低于 cmc 的低 HTA+ 濃度下,I- 也溶解在電極表面形成的 HTA+ 單層中。 在 HTA+ 單層中,I2 比 I- 更穩定。 在膠束后 HTA+ 濃度下,NP 溶液中峰電位的負移大于 β-E2 溶液。 這是因為 NP 更有效地降低了 cmc,并且在相同濃度 (0.5 mM) NP 或 β-E2 的體相中,NP 中形成的膠束量更大。 在圖 6 中觀察到的顯著吸附減少峰在圖 7a 中沒有觀察到。 然而,在圖 7b 中,在 4 mM 的 HTA+ 濃度下,在 340 mV 附近觀察到了一個寬的吸附峰。 在NP溶液中,大量膠束溶解了電極表面形成的I2,將它們從那里帶走,降低了I2的吸附峰電流。
表 3 在含有 20 mM 磷酸鹽緩沖液和 0.5 μM 芘的 50 mM hp-β-CD 存在下,HTAB 溶液在不同 NP 或 β-E2 濃度下的 cmc 值











