合作客戶/
拜耳公司 |
同濟大學 |
聯合大學 |
美國保潔 |
美國強生 |
瑞士羅氏 |
相關新聞Info
疏水劑HFBⅡ和乳清蛋白組成的混合體系中的表面流變學與泡沫歧化穩定性的關系——摘要、介紹、材料和方法
來源:上海謂載 瀏覽 906 次 發布時間:2022-02-08
摘要
在這里,我們使用朗繆爾槽研究了乳清分離蛋白(WPI)和疏水蛋白HFBII在空氣/水界面的擴散層和吸附層的表面膨脹特性,并將其與泡沫能力和穩定性聯系起來。在擴散和吸附系統中,觀察到模量隨著HFBII在表面或本體中的分數逐漸增加,我們可以確定WPI主導和HFBII主導行為的不同區域。通過目視觀察槽表面出現的微觀皺紋,進一步證實了HFBII的優勢。當比較擴散和吸附系統時,發現需要更高的HFBII分數才能在擴散層中獲得HFBII主導行為,而不是吸附層(fHFBII分別為0.6和0.2)。此外,我們的結果表明,在連續的大規模壓縮/膨脹循環中,HFBII對界面行為的貢獻變得更加顯著。為了解釋這種非平凡的行為,我們建議在界面處形成多層結構,頂層富含HFBII,底層富含WPI。泡沫的粗化穩定性與吸附層的表面膨脹特性比擴散層的表面膨脹特性更接近。最后,觀察到,在HFBII和WPI的混合體系中,粗化過程趨于平穩,這與HFBII在混合WPI:HFBII層中的主導地位隨著收縮氣泡表面發生的大表面變形而增加。
1.介紹
疏水蛋白是絲狀真菌產生的一類具有高度表面活性的蛋白質。它們的生物學功能是介導(氣生)菌絲、孢子和子實體的形成,在此過程中,親水和疏水環境(即細胞材料和空氣)之間形成一個大界面[1]。
疏水蛋白由100±25個氨基酸組成,具有8個半胱氨酸殘基的特征模式,形成4個分子內二硫鍵[2],使蛋白質分子非常緊密且堅硬。疏水蛋白的三級結構顯示出明顯的疏水區和親水區[3-5]。根據其水溶性和親水性模式,疏水蛋白可分為兩類[4]。I類疏水蛋白是最具表面活性的,但水溶性很低,因此難以在實際應用中使用。II類蛋白的表面活性略低(與1類疏水蛋白相比,但與任何其他蛋白質類相比,仍然非常出色),并具有良好的水溶性。對于II類疏水蛋白,HFBII是小分子量(7.2 kDa)和4個二硫鍵的獨特組合,可防止疏水部分重排到蛋白質核心,并使其暴露于周圍介質中。因此,在水環境中,HFBII表現為天然Janus顆粒[4],具有不同的親水性和疏水性表面補丁,從而導致不同的兩親性行為以及本體和表面自組裝。
最近,Cox等人[6]研究了HFBII的表面性質,并用其解釋了簡單氣泡團中極低的空氣溶解速率。在后續工作中,Cox等人[7]證明了HFBII可以用于生產液體泡沫,這種泡沫在幾個月內保持穩定。因此,這些分子被描述為空氣結構蛋白。這種穩定性是異常的,因為在大多數情況下,液體泡沫會通過歧化過程穩定地變粗[7,8]。正因為如此,人們往往依賴于體積彈性來穩定泡沫,從而限制了應用量,例如面包、冰淇淋或慕斯和巴瓦羅甜點[9]。
現在,HFBI穩定化泡沫中歧化的異常穩定性可以用非凡的表面性質來解釋:HFBII具有極高的解吸能,它看起來是一種致密、堅硬且粘性的顆粒[8,10]。因此,HFBII表層在振蕩和穩定膨脹狀態下都具有出色的表面剪切和膨脹模量[8,11]。此外,它們在持續壓縮時顯示出褶皺形成,這與表層的彎曲彈性有關[10]。
當將這些空氣結構蛋白應用到消費品中時,它們幾乎不可避免地會遇到其他同樣具有表面活性的成分,例如蛋白質。例如,眾所周知,混合蛋白質和/或乳化劑系統的表面性質可能與純系統的表面性質截然不同,這可能導致乳液或泡沫的穩定或不穩定[12–14]。最近,關于HFBII和-酪蛋白混合層的表面剪切流變學的數據也已公布,為此類層的分層提供了詳細的假設[15]。
為了探索其他蛋白質對HFBII作為泡沫歧化穩定劑的功能性的影響,本文致力于HFBII和乳清分離蛋白(WPI)的混合體系。在WPI中,主要蛋白質是-乳球蛋白:一種具有代表性且經過充分研究的球狀食品蛋白質,分子量約為18 kDa,等電點為5.1,在吸附到界面時能夠展開[8,16–20]。
該研究的目的是將已知成分的混合層的行為與混合物的發泡行為關聯起來。為此,我們選擇了三個步驟來接近這些極限:第一步是研究HFBII:WPI水溶液混合物層的膨脹表面性質,這些混合物分布在純空氣/水界面上,從而確定界面處蛋白質的初始組成。由于這兩種蛋白質都相對較大(它們是大分子),并且具有顯著的表面活性和附著能,因此預計不會有(或不可逆的)蛋白質脫附到整體上。因此,在壓縮/膨脹循環期間,蛋白質濃度和組成預計保持不變。在第二步中,我們使用吸附系統,制備具有已知體積組成的兩種蛋白質的水溶液,并使該系統在空氣/水中自發吸附,并與體積平衡。很明顯,在這種情況下,由于蛋白質對界面的親和力不同,體積和表面成分可能不同。當我們開始壓縮/膨脹循環以探索表面膨脹流變學時,由于多種原因,表面成分也可能發生變化。在膨脹循環期間,蛋白質可能在表面積聚,在界面和表面下重新排列,可能形成多層,在壓縮循環期間,蛋白質解吸的程度要低得多。因此,在這一過程中,系統可以在頂層富集最具表面活性的蛋白質,而在界面下方可能形成第二層的表面活性較低的蛋白質則被耗盡。此外,為了將這些與歧化穩定性聯系起來,我們選擇應用大變形膨脹流變學,并已建立和驗證了歧化的理論聯系[8,9,21]。我們的最后一步是評估混合蛋白質溶液的泡沫形成和泡沫歧化穩定性,并嘗試將泡沫特性與吸附層和鋪展層的表面膨脹流變性相關聯。
2.材料和方法
2.1.材料
II類疏水蛋白HFBII(分子量7200 Da)從芬蘭VTT生物技術公司獲得,并從里氏木霉中提取[22,23]。儲備溶液儲存在冰箱中,使用前解凍、稀釋并在超聲波浴中處理30秒。在朗繆爾槽實驗中,乳清蛋白分離物“Bipro”來自Davisco(美國),其中大部分(約50 wt%)為乳球蛋白。黃原膠Ketrol RD是從CPKelco(美國圣地亞哥)購買的。
2.2.方法
2.2.1.使用朗繆爾槽的小變形和大變形膨脹表面流變學
對于空氣/水表面的表面膨脹流變學實驗,我們使用了Kibron Inc.(芬蘭埃斯波)生產的MicroTroughX Langmuir槽。席胡氏的尺寸為230×55毫米(A=11800平方毫米),亞相體積約為15 mL。表面張力是用超靈敏的KiBron傳感器、小直徑(0.51毫米)特殊合金絲在槽的中部測量的。靈敏度優于0.01mn/m。
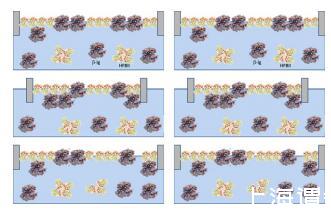
對于擴散系統,制備了1 mg/ml HFBII和1 mg/ml WPI的儲備溶液,并按不同的混合比例混合。廣泛清潔朗繆爾槽后,向槽中注入約15毫升清潔去離子(微孔)水,在真空下脫氣,屏障設置為3000 mm2。用注射器清潔屏障之間的界面后,表面擴大到10000 mm2。將表面張力探針應用于界面并進行校準。使用干凈的10μl帶針頭的玻璃微注射器,將約2μl的等分蛋白質溶液涂抹在表面的幾個點上,直到涂抹總體積為15μl。在傳播蛋白質的同時,表面壓力通常上升到大約1到3 mN/m。在平衡表面15分鐘后,以5 mm/min的線速度將面積壓縮至3000 mm2,同時記錄表面張力隨時間的變化。隨后,使用滯后函數,在5至30 mN/m的表面壓力之間(或根據系統允許的范圍進行微調)施加5次膨脹-壓縮循環。對于混合體系,每個分子的面積定義為槽面積除以所有WPI和HFBII分子的總和,并按其應用的質量進行稱重。從吸附層上拍攝照片,可以看到褶皺的形成。
為了進行吸附實驗,制備了0.1 mg/ml HFBII和0.1 mg/ml WPI的儲備溶液,并將其混合到幾種混合比例。廣泛清潔朗繆爾槽后,用5毫升移液管小心地在3000 mm2的屏障之間填充20毫升蛋白質溶液。請注意,它試圖從屏障外部填充,以確保屏障內部的初始界面干凈,但HFBII的存在會在穿過屏障時產生褶皺。用注射器清潔屏障內部的界面后,表面以140 mm/min的速度膨脹至10000 mm2,同時記錄表面張力。然后讓表面堆積1000 s,然后以5 mm/min的線速度壓縮至3000 mm2。再次膨脹至10000 mm2后,在表面壓力的最大可能范圍(例如,純HFBII為20–40 mN/m,純WPI為15–25 mN/m)之間開始5個周期的滯后函數。
使用內部開發的軟件工具計算膨脹模量。該工具首先通過使用N階切比雪夫多項式對測量的П-A曲線進行分割和平滑,從而對其進行粗略的縮減。然后使用解析樣條導數表達式對模量進行數值計算,使我們能夠計算沿實驗П–A曲線的任意點處的膨脹模量。
2.2.2.發泡實驗
250毫升燒杯裝有偏心軸,以支撐磁性攪拌裝置Nespresso Aeroccino milk frothing whisk(荷蘭當地商店購買),該裝置與恒壓直流電源相連,以避免因電池放電而導致功率和再現性損失。
在泡沫實驗中,制備了1 mg/ml HFBII和1 mg/ml WPI的儲備溶液。將儲備溶液在燒杯中按所需比例混合,使總樣品體積為100 ml。在1600 rpm下攪拌樣品6 min。由于泡沫產生后粘度增加,攪拌器偶爾會從主軸上跳下,但速度始終達到1500–1600,持續6分鐘,但有時會中斷。排水1分鐘后發現溢出。將20 ml泡沫層樣品與0.5%黃原膠溶液混合至50%的氣相體積,并使用Turbuscan(TLab Expert,Formulation,Toulouse,France)[8]實時跟蹤氣泡大小的變化約48小時。