合作客戶/
拜耳公司 |
同濟大學 |
聯合大學 |
美國保潔 |
美國強生 |
瑞士羅氏 |
相關新聞Info
不同種類的抗菌肽瓜娃素與生物膜之間的相互作用的性能對比【上】
來源:上海謂載 瀏覽 844 次 發布時間:2022-07-05
摘要
顳葉素是最早從歐洲紅蛙(Rana temporaria)的皮膚中分離出的短(10-13個氨基酸)線性抗菌肽,對革蘭氏陽性細菌和白色念珠菌有效。為了深入了解其作用機制,我們比較了該家族的兩個成員對模型膜的影響,即。,temporin B(LLPIVGNLLKSLL-NH2)和temporin L(FVQWFSKFLGRIL-NH2)。更具體地說,我們測量了它們插入脂質單分子膜以及它們對脂質體雙層結構動力學的影響,如二苯基己三烯(DPH)和芘標記的磷脂所揭示的。我們還觀察了這些肽對巨大囊泡拓撲結構的影響。這兩種時間蛋白都很容易滲透到脂質單層中,在常見細菌帶負電的磷脂-磷脂酰甘油的存在下,它們的嵌入作用增強。相反,真核細胞脂質膽固醇確實在一定程度上抵消了它們滲透到脂質膜中的作用。temporin B和temporin L均導致磷脂在雙層中富集,并且在1-棕櫚酰-2-油酰基-sn-甘油-3-磷酸甘油(POPG)存在下,這些肽增加了酰基鏈順序。Temporin B實際上對由1-硬脂酰-2-油酰基-sn-甘油-3-磷酸膽堿(SOPC)組成的巨大脂質體沒有影響,而當存在POPG時觀察到快速發泡。相反,temporin L誘導SOPC和SOPC/POPG巨囊泡形成,而SOPC巨囊泡中膽固醇的存在減弱了這種作用。
抗菌肽廣泛分布于自然界,是無脊椎動物和脊椎動物天然免疫的重要組成部分,可防止多種有害微生物的入侵和增殖。尤其是無尾類動物(青蛙和蟾蜍)的皮膚是抗菌肽的豐富來源,其結構和活性譜都具有很大的多樣性(1,2)。通常大量生產,幾種具有不同抗菌特性的不同肽通常存在于單個動物的皮膚提取物中。這種多樣性被認為對保護青蛙免受更廣泛的有害入侵者的侵害很重要(3)。蛙皮抗菌肽是在稱為顆粒腺的特殊皮膚結構中產生和儲存的,在腎上腺素能刺激或皮膚損傷時釋放其內容物。一大類不斷擴大的蛙抗菌肽,統稱為前表皮抑制素,已被證明具有高度保守的N端前序列和具有與抗菌肽對應的可變序列的C端結構域(4)。
目前,對蛙皮和其他來源的抗菌肽進行了深入研究,以闡明其作用機制。作為這項工作的結果,抗菌肽通常被認為通過滲透或破壞細胞膜的穩定性來殺死靶細胞,無論是原核細胞還是真核細胞。然而,精確的機制仍不完全清楚。關于抗菌肽與生物膜和模型膜的相互作用,最近有許多優秀的綜述,提供了迄今為止提出的用于解釋肽誘導的膜滲透過程的不同模型的完整視圖(5-8)。
顳蛋白是一類抗菌肽,首先從歐洲紅蛙的皮膚中分離出來(9)。最近,在林蛙屬其他物種的皮膚提取物中發現了顳蛋白家族的新成員,即。,R、clamitans(10)、luteiVentris(11)、pipiens(11)和grylio(12)。因此,這些發現也可以深入了解這些肽在相關物種之間的進化和分化(10,11)。顳蛋白是具有凈正電荷和酰胺化C端的線性10-13殘基長肽,在非極性溶劑(如三氟乙醇)中可能呈現兩親R螺旋構象(9,13)。發現時間蛋白A和B對大腸桿菌細胞壁缺陷突變株也有活性,并釋放脂質體包埋的熒光探針(9,13)。該家族的一個成員,時間蛋白D,對紅細胞有溶解作用(13)。最近對兩種不同的顳蛋白B對映體在糞便環境中的穩定性進行的研究表明,肽的D異構體的失活速度比L異構體慢(14)。因此,當考慮治療用途時,D異構體可能更可取。
顳蛋白與脂質的相互作用尚未得到詳細研究。為了更深入地了解這些肽的作用模式,并將其與我們實驗室先前研究過的其他兩種抗菌肽(15)馬蓋寧2和吲哚肽進行比較,我們研究了顳蛋白B(LLPIVGNLLKSLL-NH2)和顳蛋白L(FVQWFSKFLGRIL-NH2)與模型膜的相互作用。更具體地說,我們研究了它們插入脂質單層的能力,使用二苯基己三烯(DPH)1和芘標記的磷脂對脂質雙層結構動力學的影響,以及對巨大脂質體形態的影響。
材料和方法
材料。Hepes和EDTA來自Sigma。1-硬脂酰-2-油酰基-sn-甘油-3-磷酸膽堿(SOPC)、1-棕櫚酰-2-油酰基-sn-甘油-3-磷酸甘油(POPG)和–膽固醇來自Avanti極性脂質(Alabaster,AL)。熒光磷脂類似物1-棕櫚酰-2-[10-(芘-1-基)癸酰基]-sn-甘油-3-磷酸膽堿(PPDPC)來自K&V Bioware(芬蘭埃斯波)和EGA Chemie(德國斯坦海姆)的二苯基己三烯(DPH)。使用高精度電子天平(Cahn、Cerritos、CA)通過重量法測定未標記脂質的濃度,并通過341 nm處的吸光度,分別使用38000和88000 cm-1的摩爾消光系數測定含芘磷脂和DPH的濃度。在用氯仿/甲醇/水(65:25:4,v/v/v)開發的硅酸涂層板(德國達姆施塔特默克公司)上,通過薄層色譜法檢查脂質的純度。碘染色后以及在適當情況下,紫外線照射后對平板進行檢查,未發現任何雜質。合成顳葉素從塔納實驗室(德克薩斯州休斯頓)購買。通過HPLC分析肽的純度(顳蛋白B和顳蛋白L的純度分別大于90%和大于94%),并通過自動Edman降解和質譜驗證其序列。通過重量法和定量離子交換柱色譜法以及茚三酮衍生法測定肽濃度。
肽對脂質單層的滲透。使用磁力攪拌的圓形聚四氟乙烯孔(多孔板,亞相體積1.2 mL,Kibron Inc.,芬蘭赫爾辛基)測量肽插入位于空氣/水界面上的脂質單層。表面壓力(π)通過連接到連接到奔騰PC的微量天平(DeltaPi,Kibron Inc.)上的Wilhelmy線進行監測。所示脂質以氯仿(約1 mg/mL)的形式擴散到空氣/緩沖液(5 mM Hepes,0.1 mM EDTA,pH 7.0)界面上。隨后,在將temporins(0.3μM最終濃度)注入亞相之前,允許脂質單層在不同初始表面壓力(π0)下沉淀約15分鐘。注射肽后π的增量在大約30分鐘內完成,初始表面壓力(π0)與肽滲透到膜中后觀察到的值之間的差值取為?π.數據表示為?πvsπ0。這些圖還得出了與阻止肽插入膜中的脂質側向堆積密度相對應的臨界表面壓力πc。所有測量均在環境溫度下進行,一式三份(≈+24°C)。
制備大的單層囊泡(LUV)。將適量的脂質儲備溶液混合在氯仿中以獲得所需的組合物,其中PPDPC(X)0.01)或DPH(X)0.002)包括作為熒光探針。在氮氣流下去除溶劑,隨后在減壓下將脂質殘留物保持至少2小時。然后在50°C下將干脂質在5 mM Hepes、0.1 mM EDTA、pH 7.0中水合,以產生1 mM的脂質濃度。使用Liposofast低壓均質器(加拿大渥太華Avestin)通過兩個聚碳酸酯過濾器(孔徑100 nm,Bedford,MA)堆疊擠出所得分散體,以獲得平均直徑在111和117 nm之間的大單層囊泡(17)。
Ie/Im的測量。芘的輻照≈344 nm產生單體激發態,該激發態通過發射最大值為的光子松弛回到基態≈398 nm(Im),精確的峰能量和光譜結構取決于溶劑極性。如果芘的局部濃度足夠高,激發單體可能與基態芘碰撞,形成激發二聚體(準分子)。準分子通過發射以中心為中心的寬而無特征的量子帶,解離回兩個基態芘≈480納米(18,19)。用Perkin Elmer LS50B熒光光譜儀和磁力攪拌恒溫反應杯室測量用PPDPC(X)0.01)標記的LUV的熒光發射光譜。激發和發射均使用4 nm的帶寬。使用的脂質濃度為20μM,溫度保持在25°C。添加適量肽后,在記錄光譜之前,樣品平衡5分鐘。取三次掃描的平均值,并分別測量Im和Ie處的發射強度。≈取398和480 nm進行
DPH的熒光各向異性(r)。DPH在X)0.002處包含在脂質體中。使用的脂質濃度為20μM,溫度保持在25°C。使用帶有Perkin Elmer LS50B的寶麗來膜式過濾器以L格式測量極化發射。使用10 nm帶寬,在360 nm激發和450 nm發射下測量DPH的熒光各向異性r,并使用Perkin Elmer提供的軟件例程計算其值。
形成巨大脂質體。如其他地方所述(20-22)制備了巨大脂質體。將溶解在二乙醚/甲醇(9:1,v/v,濃度為1 mM)中的約1-3μL指示脂質攤鋪在兩個鉑電極的表面上,然后在氮氣流下干燥。通過在真空中抽空1小時來去除可能的有機溶劑殘留。在蔡司IM-35倒置熒光顯微鏡的工作臺上放置一個帶有連接電極和石英窗口底部的玻璃室。在添加1.3 mL pH值為7.4的0.5 mM Hepes緩沖液之前,施加交流電場(頻率為4 Hz、振幅為0.2 V的正弦波函數)。在水合作用的第一分鐘內,電壓增加到1.0 V。2小時后關閉交流電場,使用霍夫曼調制對比度(HMC)光學系統觀察到巨大的脂質體,其物鏡為10×/0.25(modulation optics Inc.,紐約)。巨大脂質體的大小是通過微管的運動校準圖像,將其作為微操作器步長(50 nm)的適當倍數(帶有MC2000控制器的MX831、SD儀器、Grants Pass或)。使用珀爾貼冷卻的12位數字CCD攝像機(C4742-95,日本濱松)與計算機連接,并通過攝像機制造商提供的軟件(HiPic 5.0.1)進行操作,記錄圖像。
微量注射技術。內部尖端二聚體>0.5μm(23)的微移液管由硼硅酸鹽毛細管(外徑1.2 mm)通過微處理器控制的水平拉拔器(P-87,Sutter Instrument Co.,Novato,CA)制成。將指示量的肽溶液(10 mM Hepes中的0.5 mM,0.1 mM EDTA,pH 7.0)施加到單個巨大脂質體的外表面,作為一系列約20 fL的單次注射,用氣動微注射器(PLI-100,Medical Systems Corp.,Greenvale,NY)輸送。為了便于操作,只使用附著在電極表面的囊泡。所有實驗均在環境溫度下進行(≈+并重復至少10次。
結果
顳葉素對脂質單層的滲透。在將配體(如肽)注射到水/氣界面上的脂質單分子膜中后,將其插入到水/氣界面上的脂質單分子膜中會導致增加?π、在表面壓力下。獲得的數據表示為?π、作為薄膜初始表面壓力的函數,π0(15,16)。表面壓力變化的幅度可用于評估肽-脂質相互作用的相對能量,并表征肽的脂質特異性(綜述見16)。先前采用該技術的研究表明,抗菌肽,如馬蓋寧2和吲哚肽,可以有效插入脂質膜(15)。同樣,顳蛋白B和顳蛋白L均有效插入脂質單層,如初始壓力(π0)為0.20)時的SOPC/POPG膜(XPOPG)所示≈15 mN/m(圖1)。然而,兩種肽表面壓力增加的動力學明顯不同。因此,在亞相中加入顳蛋白B(圖1,圖A)后,π出現快速瞬態峰值,然后是松弛,然后是π緩慢增加。這些動力學與脂質成分無關,初始表面壓力在12-36 mN/m范圍內變化。相反,對于Temporan L,表面壓力值以連續方式增加,在大約40分鐘內達到平臺(圖1,面板B)。現階段未對動力學進行更詳細的研究。
隨后從以下方面分析了來自上述類似測量的數據:?πvsπ0(圖1,面板C和D)。時間蛋白B很容易插入到高達π0的SOPC單分子膜中≈39 mN/m,其中?π-π0數據點外推到?π)0.因此,該值表示該肽不再插入SOPC單層的臨界包裝壓力πc(圖1,面板c)。與其凈正電荷+2一致,當膜中酸性磷脂POPG的含量增加時,時間蛋白B向脂質單層的滲透逐漸增強(圖1,面板C),πC的值急劇增加。有趣的是,當XPOPG在0.10和0.40之間變化時?temporin B的πvsπ0數據在表面壓力為的情況下顯示出一個“交叉”點≈32 mN/m。具體來說,在后一個表面壓力以下,增加?π隨著膜中POPG的增加而增加,而在π0>32mn/m時觀察到相反的情況。πc的值在序列中降低≈64,≈55,和≈當XPOPG分別從0.10增加到0.20和0.40時,為48 mN/m(圖1,面板E)。將膽固醇(X)0.10)包含在SOPC膜中抑制了該肽在π0處插入單層≈27 mN/m(圖1,面板C),而πC增加到≈4200萬/米。
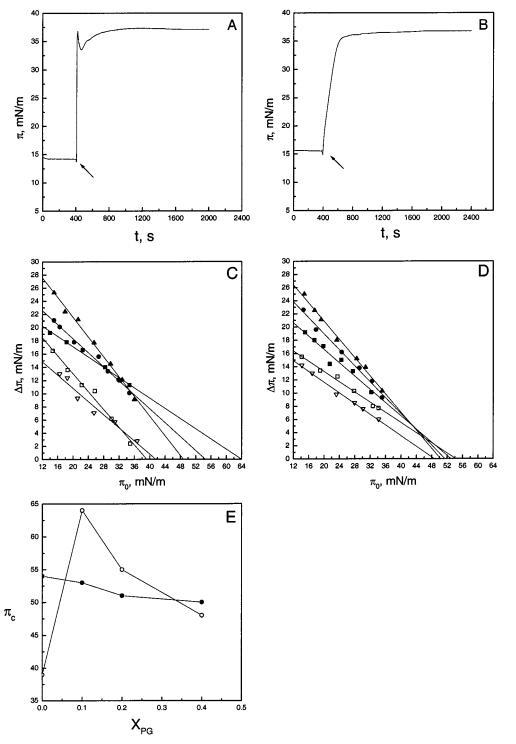
圖1:將時間蛋白B和L插入脂質單層。在初始表面壓力(π0)分別為14.6和15.5 mN/m的情況下,在SOPC/POPG(XPOPG)0.2)單層下方注射顳蛋白B(面板a)或顳蛋白L(面板B)后,表面壓力隨時間的增加而增加。肽(0.3μM最終濃度)的添加用箭頭標記。表面壓力增量(?π)將0.3μM顳蛋白B(圖C)或顳蛋白L(圖D)添加到亞相中導致的脂質單分子膜的數量表示為初始表面壓力(π0)的函數。SOPC中POPG(XPOPG)的含量分別為0(0)、0.10(9)、0.20(b)和0.40(2)。還顯示了將肽插入具有Xchol)0.1(3)的SOPC膜中。圖E顯示了πc的值,分別作為滲透時間蛋白B(O)和時間蛋白L(B)時XPOPG的函數。每個數據點代表三次測量的平均值。標準偏差在0.1和0.8 mN/m之間變化,為清晰起見,未顯示。
也觀察到由于顳蛋白L,π顯著增加,表明其滲透到SOPC單層(圖1,面板D)。然而,temporin L明顯比temporin B更具膜活性,具有πc≈54 mN/m。與temporin B類似,單分子層中POPG含量的增加增強了temporin L的滲透性,增加了?π以下≈43 mN/m(圖1,面板D)。然而,在表面壓力的后一個“交叉”值以上,由于時間蛋白L引起的π增量被POPG略微衰減,導致在存在POPG的情況下πc減小,轉移到≈53,≈51,和≈XPOPG時為50 mN/m),分別為0.10、0.20和0.40(圖1,面板E)。至于顳蛋白B,由顳蛋白L引起的π增量被膽固醇(Xchol)0.10減弱,而πc從≈54至≈48 mN/m(圖1,面板D)。
顳蛋白對雙層脂質動力學的影響。隨后通過記錄摻入LUVs的芘標記熒光磷脂類似物PPDPC(X)0.01)的發射光譜來研究肽與脂質體結合的后果。對于含有脂質類似物(如PPDPC)的單個芘部分,穩態Ie/Im值反映了膜中熒光團的橫向遷移率和局部濃度(18,19)。然而,我們之前的研究比較了兩種其他抗菌肽(馬蓋寧2和吲哚肽)對膜脂質動力學的影響,發現這些肽也影響芘標記脂質的量子產率(15)。對于SOPC LUV,添加temporin B分別導致芘單體和準分子發射Im和Ie的顯著減少,最大減少約40%(圖2,面板a和B)。芘熒光帶的猝滅是雙相的,當時間蛋白B與脂質的摩爾比約為1:12時,量子產率顯著降低(圖2,面板a和B)。在膽固醇(Xchol)0.10)存在的情況下,temporin B對芘單體和準分子熒光的猝滅也很明顯,盡管發射的減少量小于在SOPC LUV中觀察到的減少量(圖2,面板A和B)。然而,當酸性磷脂POPG存在于XPOPG)0.10時,Im中只有微不足道的變化是明顯的,當XPOPG從0.20增加到0.40時,時間蛋白B導致Im以漸進的方式增加,Im的初始增量在大約2/1的POPG/時間蛋白B化學計量比下趨于穩定。在達到飽和響應之前,Im中線性增量的斜率隨著XPOPG而增加(圖2,面板C)。在POPG存在的情況下,顳蛋白B也增加了Ie。在XPOPG)0.40時,Ie的值逐漸增加,直到顳蛋白B:脂質摩爾比為≈1:15,對應于≈1/6,而當超過該化學計量比時,Ie降低。圖3,面板A中顯示了由于顳蛋白B引起的Ie/Im的變化。具體而言,SOPC LUV的Ie/Im增加了1.1倍,而在膽固醇(Xchol)0.10的存在下,觀察到Ie/Im的微小變化,面板A)。將XPOPG從0.10增加到0.20會逐漸增強Ie/Im的增量。有趣的是,在XPOPG)0.40時,當時間蛋白B:脂質摩爾比為≈1:30.然而,在這一肽:脂比之上,顳葉素B導致Ie/Im降低,而在這一肽:脂比之上,Ie/Im的變化不顯著≈1:6.
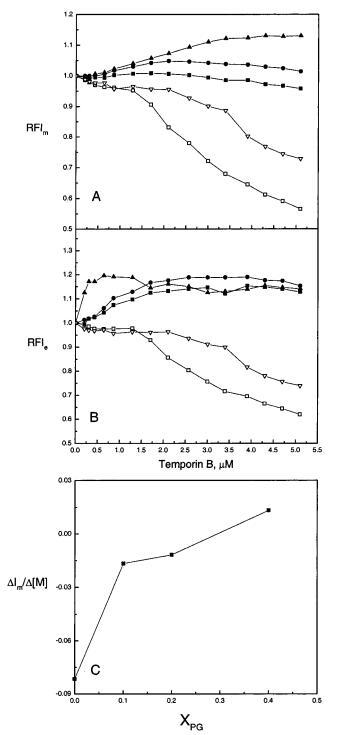
圖2:通過芘標記的磷脂PPDPC(X)0.01的熒光評估顳葉素B對LUV中脂質動力學的影響,分別顯示為芘單體和準分子發射強度Im(圖A),Ie(圖B)的變化,以及在RFIm中達到飽和反應之前Im增加的斜率(圖C)。脂質體由SOPC組成,XPOPG為0(0)、0.10(9)、0.20(b)和0.40(2),Xchol為0.10(3)。總體積為2 mL的5 mM Hepes,0.1 mM EDTA,pH 7.0,脂質濃度為20μM。使用循環水浴將溫度保持在25°C。每個數據點代表三次測量的平均值。標準偏差小于0.02(面板A和B)和0.004(面板C),為清晰起見,未顯示。
芘標記的脂質PPDPC的Ie/Im增強通常被評估為是由于探針的側向分離或脂質側向擴散速率增加所致。為了解決這兩種相互非排斥機制之間的矛盾,我們測量了膜中DPH的穩態熒光各向異性r(圖3,面板B)。DPH是一種小的、疏水的桿狀熒光團,其中很大一部分位于雙層的碳氫化合物區域,平行于膜脂的長軸。其發射各向異性可用于評估酰基鏈順序(有關綜述,請參閱24)。增加脂質堆積后,觀察到酰基鏈順序增加,從而減少脂質側向擴散(25,26)。顳葉素B對SOPC和SOPC/膽固醇(Xchol)0.10)LUVs的r僅產生了微不足道的變化(圖3,面板B)。因此,SOPC-luv的酰基鏈順序沒有變化以及Ie/Im的增加表明PPDPC很可能富集到微域中。隨著XPOPG的增加,添加顳蛋白B后,脂質堆積和酰基鏈順序逐漸增強。因此,膜橫向擴散的增加不能導致觀察到的Ie/Im和顳葉素B誘導的脂質分離的增加;即。,可以得出PPDPC在膜中聚集的結論。然而,當考慮淬火過程的影響時,解釋變得更加復雜。
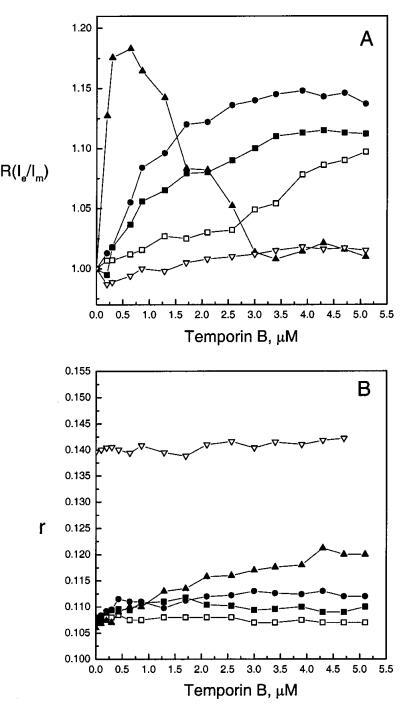
圖3:通過芘標記的磷脂PPDPC(X)0.01)的熒光和DPH(X)0.002的穩態發射各向異性r評估顳葉素B對LUV中脂質動力學的影響,顯示為具有XPOPG)0(0)、0.10(9)、0.20(B)和0.40(2)的SOPC脂質體中歸一化準分子與單體比率r(Ie/Im)(圖A)和各向異性r(圖B)的變化,Xchol)0.10(3)。每個數據點代表三次測量的平均值。標準偏差小于0.02(面板A)和0.004(面板B),為清楚起見,未顯示。否則情況如圖2圖例所示。

圖4:通過芘標記的磷脂PPDPC(X)0.01的熒光評估顳葉素L對LUV中脂質動力學的影響,分別顯示為芘單體和準分子發射強度Im(圖A)和Ie(圖B)的變化。脂質體由SOPC組成,XPOPG為0(0)、0.10(9)、0.20(b)和0.40(2),Xchol為0.10(3)。每個數據點代表三次測量的平均值。標準偏差小于0.02,為清晰起見,未顯示。否則情況如圖2圖例所示。










