合作客戶/
拜耳公司 |
同濟大學 |
聯合大學 |
美國保潔 |
美國強生 |
瑞士羅氏 |
相關新聞Info
DEAE-瓊脂糖LB膜的制備方法、最佳成膜濃度及表面電勢測定
來源:生物學雜志 瀏覽 30 次 發布時間:2024-07-08
由于單分子膜性能獨特,受到關注度越來越高,利用LB膜技術制備了二乙氨乙基(DEAE)-瓊脂糖單分子層。分析其表面壓(π)-面積(A)曲線,崩潰壓較高,成膜過程明顯。研究濃度對DEAE-瓊脂糖成膜情況的影響,確定最佳成膜濃度為0.5 mg/mL。考察配基密度與表面電勢的關系,其表面電勢隨著配基密度的增加而增大。采用原子力顯微鏡(AFM)和布魯斯特角顯微鏡(BAM)對制備的LB膜進行了表征,得出表面膜的表面平整、緊密,厚度約為7.9 nm。DEAE-瓊脂糖LB膜制備成功,為以后LB膜技術的廣泛應用提供了一種新的材料。
近年來,隨著分子技術的不斷發展,人們對分子水平材料的關注度越來越高,這就包括單分子膜制備技術。單分子膜應用十分廣泛,如傳感器、檢測器、非線性光學器件的制備以及生物薄膜的簡化模擬等。利用單分子膜在分子水平對材料進行制備和研究,已經成為最近的熱門課題。
常用的制備單分子膜方法主要有分子自組裝和Langmuir-Blodgett(LB)膜技術兩種。分子自組裝是構膜分子通過分子間及其與基底材料間的物化作用而自發形成的一種熱力學穩定、排列規則的單層(或多層)分子膜[1]。張一芳等[2]在金電極表面自組裝1,6-己二硫醇(HDT)單分子膜,通過納米金與巰基間的金硫鍵(Au-S)作用組裝一層金納米顆粒構建傳感界面,作為電化學免疫傳感器用于瘦肉精——克倫特羅(CL)的檢測。馬翠翠[3]研究了基于紫外光降解自組裝單分子層的紙芯片及其應用。LB膜技術是在室溫條件下,將兩親性分子在氣液界面上施加橫向壓力使其有序排列,最后將單分子薄膜轉移到特定固體基底表面的薄膜制備技術[4]。Zou等[5]利用LB膜技術制備了納米金顆粒和聚苯胺單分子薄膜作為化學傳感器,用于尿酸和腎上腺素的檢測。Lee等[6]制備了基于鈀納米顆粒的單壁碳納米管LB膜,作為一種氫氣傳感器。白燁[7]利用LB膜技術制備帶有功能性基團的寡聚對苯撐乙烯(OPV)制備單分子層薄膜,為開發有機光電分子器件奠定了一定的基礎。相對于分子自組裝來說,LB膜技術的優點在于制備的單分子層膜厚度可控制到分子級甚至納米級,成膜物分子排列取向可控,成膜條件簡單,不需要破壞成膜材料的結構,轉移方式簡便,利于后續修飾或偶聯等[8-10]。
多糖類物質作為一種生物大分子,其研究應用一直是人們關注的熱點[11-12]。在醫藥領域中,改性后納米纖維素可以應用于疏水性藥物的傳遞[13],改性后的羥乙基纖維素(HEC)與透明質酸(HA)結合應用于研究異甘草素的透皮給藥[14],改性后的瓊脂糖可以用于抗癌藥物實驗[15]。在生化領域中,改性后的DEAE-瓊脂糖可以作為一種層析分離介質的重要基質,具有硫酸根含量低、凝膠強度高、電內滲低等性能[16-17],廣泛應用于凝膠電泳、層析分離和免疫學研究等方面[18]。DEAE-瓊脂糖作為一種生物高分子化合物,適用于單分子膜的制備[19],可以為單分子層膜的發展應用提供一種新型材料。
本研究擬制備改性的DEAE-瓊脂糖LB膜,優化鋪展溶劑,測定其面積-表面壓曲線,確定最佳成膜濃度,研究不同配基密度對表面電勢的影響,利用AFM、BAM對其進行表征,建立DEAE-瓊脂糖LB膜的制備方法,為單分子層研究提供新的資源。
1材料與方法
1.1材料與儀器
1.1.1材料
瓊脂糖購自普洛麥格(北京)生物技術有限公司,單晶硅片(晶向為N[100])購自北京中科科儀技術發展有限責任公司,其他試劑均為市售分析純。
1.1.2儀器
LB膜分析儀,KN芬蘭Kibron公司MicroTrough;原子力顯微鏡(AFM);小型布魯斯特角顯微鏡(BAM),瑞典百歐林科技有限公司。
在各功率一定時,隨著臭氧發生器出氣流量的增大,臭氧的濃度隨之減小,這主要是由于流量越小時,氧氣在臭氧發生器里的停留時間就越久,有利于臭氧的產生,并且各曲線呈現出斜率相似的趨勢,說明氧氣的濃度與氧氣在臭氧發生器的停留時間基本成正相關,但同時應考慮流量越小時,相同功率下反應器內的溫度比更大的出氣流量有所增高,會促進臭氧分解,因此,建議出氣流量不低于30Nm3/h。與此同時,臭氧的產量卻隨著流量的增大而增大,這主要是由于出氣流量在臭氧產量中所占比重更大,同時由于臭氧濃度與出氣流量的變化曲線均為線性,因此,各臭氧產量隨流量變化的曲線也呈現出線性關系。
1.2實驗方法
1.2.1 DEAE-瓊脂糖制備
將1 g瓊脂糖粉加入到50 mL水中,加熱攪拌使其全部溶解。取6 mL熱溶液于三角瓶中,加入等體積14%的NaOH溶液,同時加入1 mg NaBH4,50℃搖床堿化40 min后加入2.06 g DEAE繼續反應1 h,反應結束后,35℃透析至中性,凍干。
1.2.2硅片的處理
將1 cm×1 cm的硅片用乙醇、丙酮和超純水分別超聲波清洗各5 min,以除去硅片表面的有機雜質和水溶性雜質。將清洗好的硅片浸泡在新配制“Piranha”溶液(98%硫酸與30%的H2O2體積配比7∶3)中2 h,溫度為90℃,使硅片表面產生硅羥基端,然后用大量超純水超聲波清洗[20]。
1.2.3 LB膜制備
在室溫下,亞相為超純水,滴加300μL DEAE-瓊脂糖溶液(正丁醇,0.5 mg/mL),揮發1.5 h,壓膜速率為5 mm/min。
1.2.4 LB膜提拉
1.2.5原子力顯微鏡
沉積在硅片上的薄膜用原子力顯微鏡間接接觸模式進行檢測,范圍由大到小進行掃描,圖像由NanoScope Analysis軟件進行處理。
2結果與討論
2.1鋪展溶劑的篩選
通過性質比較、實驗測試,篩選不同的鋪展溶劑,最終選取正丁醇為鋪展溶劑。鋪展溶劑的作用是使亞相上的分子隨著鋪展溶劑在亞相表面的擴展揮發,分子均勻分布在亞相表面。鋪展溶劑應具有良好的揮發性和不溶于亞相這兩個特性。常用的鋪展溶劑有氯仿、甲醇等。然而,由于瓊脂糖DEAE化之后增加了親水性,不溶于氯仿等常用鋪展溶劑,經過篩選后使用正丁醇作為鋪展溶劑。正丁醇能溶解DEAE-瓊脂糖,同時難溶于水,揮發性較好,符合鋪展溶劑所需條件。考慮到正丁醇的揮發性遠遠不如氯仿等溶液,按照制備LB膜的方法僅在亞相上滴加正丁醇,獲得其面積-表面壓曲線,并與滴加DEAE-瓊脂糖-正丁醇溶液的進行比較,結果見圖1。從圖1中可以看出,與DEAE-瓊脂糖溶液的表面壓-面積曲線相比,正丁醇在相同時間內表面壓變化非常小,可以忽略不計,因而,正丁醇是一種適合DEAE-瓊脂糖的鋪展溶劑,經揮發后可使DEAE-瓊脂糖均勻分布在亞相表面。
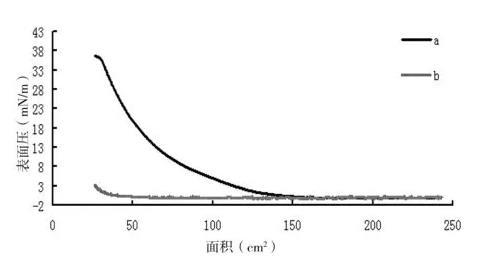
圖1面積-表面壓圖像
a:滴加DEAE-瓊脂糖-正丁醇溶液;b:只滴加正丁醇
2.2朗格繆爾膜成膜過程
2.2.1朗格繆爾膜表面壓-面積圖像
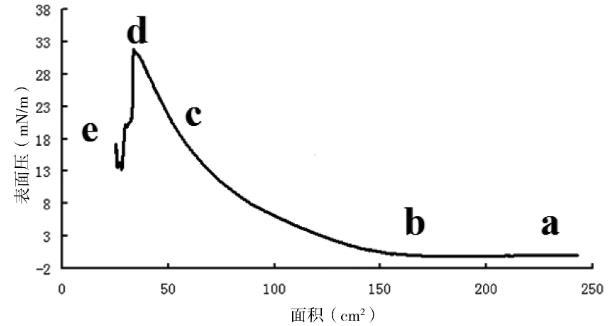
圖2 DEAE-瓊脂糖LB膜的表面壓-面積曲線(0.5 mg/mL,300μL)
利用LB膜分析儀研究了DEAE-瓊脂糖LB膜成膜面積-表面壓圖像,得出DEAE-瓊脂糖LB膜的表面壓-面積曲線(圖2)。結果表明DEAE-瓊脂糖LB膜制備成功。一般來說,朗格繆爾膜的形成過程中會出現氣態、液態和固態這3種形態,成膜之后再壓縮則會出現崩潰。從圖2中可以看出,在DEAE瓊脂糖成膜過程中,a點DEAE-瓊脂糖溶液剛剛被滴加在亞相表面上,此時DEAE-瓊脂糖分子間距較遠,在亞相表面呈分散狀態鋪散開來,每個分子所占面積較大,分子呈氣相狀態,表面壓幾乎為零。經過一定的揮發時間后,滑障從b點開始緩緩壓縮,隨著滑障的壓縮分子之間距離逐漸變小,每個分子所占面積隨之變小,表面壓開始緩緩上升,呈液相狀態。滑障壓縮一段時間后,DEAE-瓊脂糖間距變得相對較小,開始由液態向固態轉變,到達途中的c點。此時繼續壓縮,DEAE-瓊脂糖分子間距快速減小,分子之間排列緊密,每個分子所占平均面積很小,表面壓上升較快,基本形成固相狀態的單分子膜。此時繼續壓縮,固相狀態保持到d點時到達其崩潰壓力,分子間距到達最小值,表面壓升至最高,再壓縮則會破壞所形成的固相單分子層,出現瞬間崩潰。經分析看出,DEAE-瓊脂糖LB膜的成膜過程與其他材料成膜過程符合,是標準的朗格繆爾膜成膜過程,可為后續實驗鋪墊一定的基礎。
2.2.2不同濃度DEAE-瓊脂糖朗格繆爾膜制備

圖3不同濃度DEAE-瓊脂糖表面壓-面積曲線
a:0.15 mg/mL;b:0.5 mg/mL;c:1.0 mg/mL
利用LB膜儀制備了不同濃度的DEAE-瓊脂糖單分子膜,研究了其性質,圖3為不同濃度DEAE-瓊脂糖表面壓-面積圖像,結果表明成膜的最佳濃度為0.5 mg/mL。濃度為影響成膜條件的一個重要參數,通過對圖像結果分析得知DEAE-瓊脂糖朗格繆爾膜穩定性隨著溶液濃度的增加先變大后減小。從圖3中可以看出,溶液濃度為0.15 mg/mL時,表面壓不斷上升,沒有達到穩定的固相狀態,這種情況下沒有形成可提拉的固相膜。直至濃度增加到0.5 mg/mL時,出現相對穩定的表面壓,約為35~37 mN/m,在此區域內單分子膜為固相狀態,性質穩定,易于將其提拉到基片上。之后再增加溶液濃度到1.0 mg/mL,相對穩定的固相區域沒有出現,不能形成穩定可提拉的條件。對于此結果的產生可能有以下原因:當溶液的濃度很低時,在滴加量相同的條件下,所滴加在亞相上的分子數量較少,壓縮到最后,分子間距變小,但由于分子數量有限,每個分子所占面積相對較大;提高溶液的濃度到一定范圍,滴加在亞相上的分子數量變多,隨著滑障的壓縮分子之間不斷靠攏,形成穩定的單分子層固相區域,再壓縮直到分子間距到達臨界狀態,不能承受滑障壓力,出現斷裂堆層,固相區域瓦解崩潰,表面壓迅速下降;此后再提高溶液的濃度,亞相上的分子數量過多,分子之間分散不完全,在壓縮過程中可能出現堆層現象,不能形成穩定的固相區域。據此分析,制備DEAE-瓊脂糖LB膜最佳濃度為0.5 mg/mL。
2.2.3 BAM結果
利用BAM研究了DEAE-瓊脂糖單分子膜的成膜過程,圖4為表面壓為0 mN/m和34 mN/m的BAM圖像結果。通過對BAM圖像的觀測,可以看出其成膜過程,確定其是否成膜。圖4-a為DEAE-瓊脂糖剛滴加在亞相上的BAM圖像,分子被平鋪在亞相表面,相對分散,呈氣相狀態,此時布魯斯特角的折射不受表面分子影像,圖像顏色較深,看不出分子的具體形態。待其揮發一定時間后,隨著滑障的持續壓縮,DEAE-瓊脂糖由分散狀態到聚集成膜,最后在亞相上形成相對穩定的固相區域。圖4-b為固相狀態下的DEAE-瓊脂糖單分子膜,可以看出此時分子之間排列緊密,分子間距較小,已經形成固相狀態。由于分子在亞相表面緊密排列形成了單分子層,改變了布魯斯特角的折射,使得圖像的顏色變淺。通過對表面壓為0 mN/m和34 mN/m的BAM圖像對比可以看出,DEAE-瓊脂糖分子由一開始的分散狀態到達最后穩定的固相狀態,成功形成了穩定的便于提拉的單分子層。
2.3 DEAE瓊脂糖朗格繆爾膜表面電勢
利用表面電勢分析儀研究了不同配基密度對LB膜表面電勢的影響,圖5為不同配基密度DEAE-瓊脂糖LB膜表面電勢圖像。結果表明隨著配基密度的增加其表面電勢不斷增加,LB膜性質越穩定。
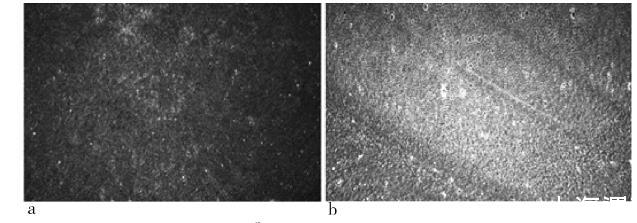
圖4表面壓為0 mN/m和34 mN/m的BAM圖像
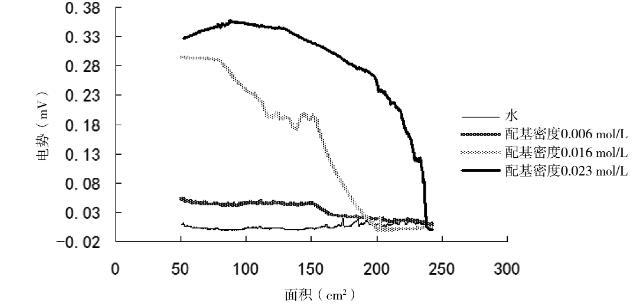
圖5不同配基密度DEAE-瓊脂糖LB膜表面電勢
表面電勢的測定可以看出不溶膜是否均勻以及其性質是否穩定。亞相表面有不性溶膜的存在,這便會引起水面上電勢的變化,因而固-液表面成膜前后有電勢差ΔV生成。成膜分子剛滴加在亞相上時,分子之間間隔相對較大,表面電勢相對較小;隨著劃障的不斷壓縮,分子越來越聚集,每個分子帶有一定的電荷數,相同檢測面積下表面電勢隨著分子的增多逐漸增大;之后亞相上的分子被壓縮到一定程度時會形成穩定的單分子層,此時分子之間距離非常小,且趨于穩定狀態,電勢差不發生很大變化。從圖5可以看出,在配基密度非常小的時候,每個分子所帶的電荷數較小,在壓縮過程中產生的電勢差非常小,基本可以忽略不計。但將配基密度增大,隨著滑障的壓縮,DEAE瓊脂糖單分子層排列越緊密,產生了一定的電勢差,在到達固相區域后相對穩定。隨著配基密度的增加,DEAE-瓊脂糖所帶的配基增多,每個分子所帶的電荷數增多,隨著滑障壓縮到一定區域,在相同檢測面積下總的分子量不變但電荷數增多,使得電勢差變大,進而表面電勢變大。隨著配基密度的增大,單分子膜性質越來越穩定。
2.4 LB膜的AFM表征
利用AFM對DEAE-瓊脂糖LB膜性質進行研究。圖6為空白硅片與DEAE-瓊脂糖LB膜的AFM 3D圖像,結果表明制備的DEAE-瓊脂糖LB膜性質較好。從AFM圖像中可以直觀看出其表面形貌,如若其表面相對平坦,無孔存在,厚度相對均勻,則可表明其制備成功。圖6-a為空白硅片的AFM圖像,硅片清洗后表面潔凈,觀測不到雜質存在。除此之外,空白硅片表面平整,厚度約為1.3 nm,可以作為DEAE-瓊脂糖LB膜提拉的基片。采用垂直提拉法將DEAE-瓊脂糖LB膜轉移到干凈硅片上,進行AFM檢測,掃描范圍由大到小。通過圖6-b可以看出,轉移到硅片上的單分子層呈平鋪狀態,分子分散均勻,膜的表面相對平坦,觀察不到有孔存在,厚度相對均勻。通過空白硅片的高度約為1.3 nm,膜沉積后的硅片高度為9.2 nm,可以估算出DEAE-瓊脂糖LB膜的厚度約為7.9 nm。這與之前報道的納米微晶纖維素LB膜的厚度是7.2 nm相符合[21]。通過軟件測得DEAE-瓊脂糖LB膜表面粗糙度Ra(輪廓算術平均偏差)為2 nm,表明膜的表面雖不完全平坦,但相對均勻。通過以上分析可以得出,DEAE-瓊脂糖LB膜制備成功,性質穩定并且被成功轉移到硅片上。
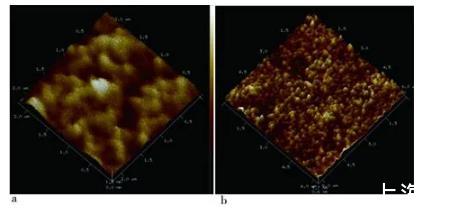
圖6空白硅片(2μm×2μm)與DEAE瓊脂糖LB膜(6μm×6μm)AFM 3D圖像
3結論
DEAE-瓊脂糖作為一種新型LB膜材料,可應用于生物大分子性能研究、藥物制劑改良、新型生物功能器件研發等多個方面。為了制備新型的DEAE-瓊脂糖LB膜,篩選了正丁醇作為鋪展溶劑,使得瓊脂糖能夠在亞相上鋪展,具備形成LB膜的基本條件;發現DEAE-瓊脂糖朗格繆爾膜成膜過程與標準成膜過程相符合;確定了DEAE-瓊脂糖朗格繆爾膜的最佳成膜濃度為0.5 mg/mL。采用BAM觀測,可以看出分子之間排列緊密,形成一層不溶性薄膜;發現隨著DEAE配基密度的增加,其表面電勢逐漸增加。將DEAE-瓊脂糖LB膜提拉到硅片上利用AFM對其進行表征,觀察到分子之間排列緊密,表面粗糙度Ra為2 nm,估算出其厚度約為7.9 nm。以上結果表明,成功制備出性質穩定的DEAE-瓊脂糖LB膜。










