合作客戶/
拜耳公司 |
同濟大學 |
聯合大學 |
美國保潔 |
美國強生 |
瑞士羅氏 |
相關新聞Info
推薦新聞Info
-
> 定性分析聚合物界面張力與系統黏度比之間的關系——數值仿真結果、結論
> 定性分析聚合物界面張力與系統黏度比之間的關系——數值模擬、實驗研究結果
> 定性分析聚合物界面張力與系統黏度比之間的關系——實驗部分
> 探究LB復合膜的酸致變色特性
> 受磷脂雙分子層啟發構建ZIBs兩性LB膜——制備高性能碘正極新思路
> 納米活性顆粒表面潤濕性測量方法及具體操作步驟
> 人工沖洗升級為超聲波清洗,可改善新能源電池沖壓配件的表面張力
> LB法組裝Silicalite-1型分子篩晶粒層,制備出高度b-軸取向的ZSM-5分子篩膜
> 微量天平高靈敏測定雞肉中磺胺類藥物含量
> 超低軌衛星環境效應研究也會用到超微量天平?
Delta-8使用新方法測試CMC,而不是表面張力測試法——討論、致謝!
來源:Unisense 瀏覽 1332 次 發布時間:2021-09-03
討論
在這里,我們提出了一種新穎的、高通量的、基于非細胞的使用熒光法預測PLD的體外篩選方法通過監測磷脂的CMC進行探測,有無與測試物品的交互。而朗繆爾平衡方法27提供了通過CMC評估PLD的可靠途徑轉變,當前的熒光方法提供了一種獨特的替代方法本機用于預測PLD風險。這種與微孔板兼容的平臺形式更具成本效益,更易于操作,具有更高的通量,可修改用于早期藥物的PLD風險評估發現。所選的熒光探針Prodan適用于脂質和測試的CMC測定形成膠束的化合物。我們清楚地證明了體內與體外或基于非細胞的對比與細胞檢測相關性使用當前方法,總體一致性為91%當應用合適的截止值(CMCDL/CMCL=0.75 in本試驗)。與兩個in silico模型相比,這更好我們也應用于我們的驗證集,其一致性Ploemen19和Tomizawa20模型的值分別為76%和80%,分別。敏感性(PLD誘導物鑒定為陽性)和選擇性(非PLD誘導劑鑒定為陰性)模型分別為92%和90%,也優于兩種計算機模型(表3)。硅片和體外分析利用了測試的固有物理化學特性使它們對磷脂更親和的化合物pids;然而,體外模型也可以確定藥物濃度對藥物脂質相互作用的影響可通過計算機模型進行預測。此外,空間化學分子和電荷的空間分布及其極性和非極性部分可以在反應性中發揮作用測試化合物和這些因素沒有被硅膠模型。此外,這個體外模型正確分配慶大霉素和紅霉素等非CAD藥物的PLD誘導潛力,因為體外模型評估了總體因此,測試化合物和脂質之間的相互作用是比硅模型更先進。反之,對于化合物在所需測試濃度下存在溶解度問題,另一種選擇應確定溶劑,否則數據可能會產生誤導。在硅膠模型沒有這個障礙,可以應用于任何具有明確結構的化合物。
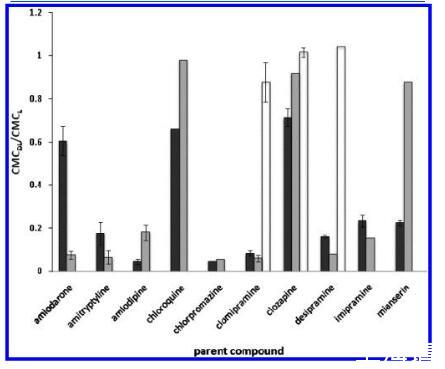
圖5.CMC偏移(由CMC之間的比率表示)藥物-脂質復合物(DL)和單獨脂質的CMC(L):CMCDL/CMCL)的測試化合物(黑色)及其主要代謝物(灰色、初級代謝物;白色,次生代謝物)在pH 7.2中分析HEPES緩沖液。使用的藥物濃度為1 mM,除非另有說明見表2。誤差線被分配給那些n g3測試的化合物。對于氯氮平和米安色林,均為0.91和0.091 mM用于測試,但僅來自1 mM測試的數據被策劃。
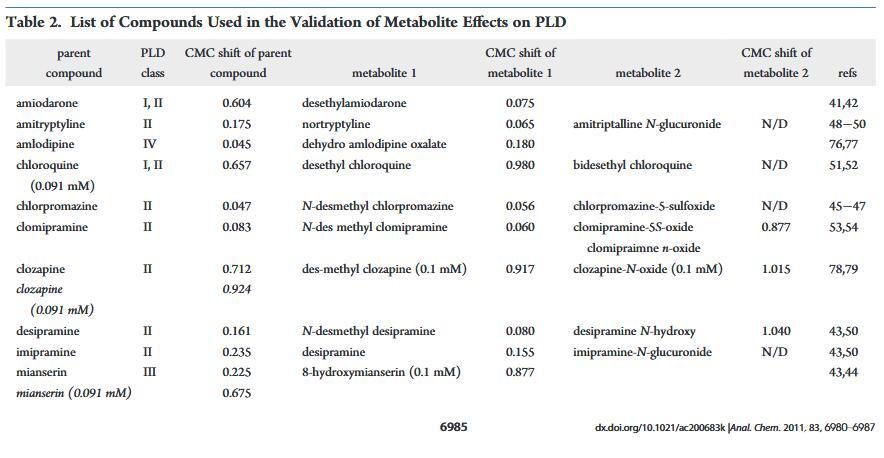
表2
據報道,藥代動力學對PLD有影響,因為劑量、24、33、36代謝、32、37?39和處置10該藥物均影響體內PLD的嚴重程度。創建一個成功的候選人需要清楚地了解PLD的原因,從而重新設計化學結構或評估合適的治療窗。
PLD所需的最低劑量不同于磅到復合,有時取決于性別。24將體內劑量與體外試驗濃度直接掛鉤可能具有挑戰性,因為藥物的血漿濃度可能受其滲透性、溶解性、代謝、所用賦形劑、給藥途徑、用藥頻率攝入量等等。但通過監測濃度測試分子對PLD能力的依賴性,即不太可能是線性的,如圖4所示,并且很難估計,我們可以確定之間的潛在關系劑量和脂質結合,從而評估安全窗口體內試驗數量有限。
已經有許多出版物描述了PLD藥物代謝產物所致。其中,初級代謝輕的胺碘酮,去乙基胺碘酮,已經討論過14,38-40優先積累代謝物已觀察到胺碘酮過量,尤其是短期39這為我們的檢測數據提供了可能的解釋其中去乙基胺碘酮是胺碘酮的主要代謝物,41,42表現出更高的PLD誘導潛力。相似地,8-羥基米安色林之間的CMC位移差異,米安色林、43,44和米安色林的主要氧化代謝物比其他兩個之間的差異更顯著成對的親本和代謝物。由于溶解度的限制,父母和代謝組的劑量濃度不同氯氮平和米安色林。這可能是導致觀察到的CMC偏移的顯著差異母體和代謝物之間。在較低濃度下測試時相比之下,氯氮平從低電位誘導劑轉變為非誘導劑,而米安色林仍然作為誘導劑但具有更高的CMCDL/CMCL值。值得注意的是,目前測試集中的大多數CAD被報告為氧化代謝其相應的脫烷基初級代謝物。為了了解相應初級的PLD電位代謝物,我們測試了額外的代謝物。之間測試的代謝物是初級去甲基代謝物氯丙嗪、45?47阿米替林、48?50丙咪嗪、43,50和pri-氯喹的瑪麗和次級脫乙基代謝物。51,52此外,由雜原子氧化形成的氧化代謝物地昔帕明43,50和氯胺酮的重釋和脫烷基代謝物pramine53,54進行了評估。與其他CAD一樣,代謝物可以如果它們具有合適的理化性質,則誘導PLD。32相反,代謝物將失去結合能力如果CAD特征丟失,則使用脂質,例如用脂質觀察氯米帕明N-氧化物和地昔帕明N-羥基(圖4和表2)。
表3

眾所周知,流通的水平和時間可能不同的代謝物以及從一種藥物到另一種藥物的變化;然而,循環的量(以摩爾計)或劑量當量代謝物可能永遠不會大于給藥的代謝物特雷德藥。在本研究中,代謝物在與他們的父母相比,相同或更低的濃度基于它們的溶解度。應該注意的是該檢測是作為一種前瞻性篩選工具而開發的;那里-因此,基本前提是測試代謝物在與母體濃度相同。在以下情況下代謝物的PLD潛力值得關注,濃度可以與相關元進行相關研究博萊特。然而,這樣的研究超出了該研究的范圍。目前的調查。層狀體的識別通過透射電子顯微鏡(TEM)是第一個適應癥溶酶體參與PLD9并表明溶酶體pH值可能是一個關鍵因素;20然而,最初沒有直接溶酶體受累的起源和功能的證據。3 A Max field和MacGraw進行的研究表明在存在下形成的內體的快速隔離變成溶酶體的磷脂生成藥物;55然而,它溶酶體的酸性pH值可能會改變脂質和目標藥物之間相互作用的嚴重程度溶酶體包涵體的形成。由于這些原因,我們相信研究這兩種pH條件是有價值的,因此獲得更全面的風險評估。在我們的驗證集中,大多數化合物在pH 7.4和4.8除了米安色林、胺碘酮和華法林,以及所有這三種通過不同的體內和實驗證明化合物是PLD誘導劑細胞檢測。
該測定顯示出高重現性和可預測性。類似于其他無法替代體內的體外測定確認結果的測量,這更便宜,更少耗時的熒光方法可以提供有用的有關藥物與脂質相互作用的早期信息。此外,這種方法可用于對候選人進行排名,協助藥物設計,并估計潛在風險。
AUTHOR INFORMATION
Corresponding Author
*Phone:617-871-7143.E-mail:LipingX.Zhou Novartis.com.
Present Addresses
§Department of Chemistry,University of Colorado-Denver,Denver,CO 80205.
ACKNOWLEDGMENT
We would like to thank Dr.Pavel Landsman for his insight on?uorescent dye probe selections,design of the experiments,and helpful discussions.Our thanks also go to Mr.Alan Bushey from Novartis IT for development of the data processing Microsoft Excel worksheet.
REFERENCES
Nelson,A.A.;Fitzhugh,O.G.Arch.Pathol.1948,45(4),454–462.
Hostetler,K.Y.;Reasor,M.;Yazaki,P.J.J.Biol.Chem.1985,260(1),215–219.
Kodavanti,U.P.;Mehendale,H.M.Pharmacol.Rev.1990,42327–354.
Vanhaelst,U.J.G.M.;Elving,L.;Hoefnagels,W.Ultramicro-scopy 1986,19(1),107–108.
Schneider,P.Arch.Toxicol.1992,66(1),23–33.
Halliwell,W.H.Toxicol.Pathol.1997,25(1),53–60.
Reasor,M.J.;Hastings,K.L.;Ulrich,R.G.Expert Opin.Drug Saf.
2006,5(4),567–583.
Martin,W.J.;Kachel,D.L.;Vilen,T.;Natarajan,V.J.Pharmacol.Exp.Ther.1989,251(1),272–278.
(9)Anderson,N.;Borlak,J.FEBS Lett.2006,580(23),5533–5540.
Hanumegowda,U.M.;Wenke,G.;Regueiro-Ren,A.;Yorda-nova,R.;Corradi,J.P.;Adams,S.P.Chem.Res.Toxicol.2010,23(4),749–755.
Reasor,M.J.;Castranova,V.Exp.Mol.Pathol.1981,35(3),359–369.
Reasor,M.J.;Walker,E.R.Exp.Mol.Pathol.1981,35(3),370–379.
Pelletier,D.J.;Gehlhaar,D.;Tilloy-Ellul,A.;Johnson,T.O.;Greene,N.J.Chem.Inf.Model.2007,47(3),1196–1205.
Sun,E.L.;Petrella,D.K.;McCloud,C.M.;Cramer,C.T.;Reasor,M.J.;Ulrich,R.G.In Vitro Toxicol.1997,10(4),459–470.
Watanabe,Y.;Watanabe,K.;Tashiro,I.;Enomoto,Y.
J.Electron Microsc.1971,20(3),255.
Tashiro,Y.;Watanabe,Y.;Enomoto,Y.Acta Pathol.Jpn.1983,33(5),929–942.
Monteith,D.K.;Morgan,R.E.;Halstead,B.Expert Opin.Drug Metab.Toxicol.2006,2(5),687–696.
Nonoyama,T.;Fukuda,R.Toxicol.Pathol.2008,21(1),9–24.
Ploemen,J.P.H.T.;Kelder,J.;Hafmans,T.;Van De Sandt,H.;van Burgsteden,J.A.;Salemink,P.J.M.;Van Esch,E.Exp.Toxicol.Pathol.2004,55(5),347–355.
Tomizawa,K.;Sugano,K.;Yamada,H.;Horii,I.J.Toxicol.Sci.
2006,31(4),315–324.
Laurent,G.;Carlier,M.B.;Rollman,B.;Vanhoof,F.;Tulkens,P.Biochem.Pharmacol.1982,31(23),3861–3870.
Nioi,P.;Perry,B.K.;Wang,E.J.;Gu,Y.Z.;Snyder,R.D.
Toxicol.Sci.2007,99(1),162–173.
Morelli,J.K.;Buehrle,M.;Pognan,F.;Barone,L.R.;Fieles,W.;Ciaccio,P.J.Cell Biol.Toxicol.2006,22(1),15–27.
Miyamoto,S.;Matsumoto,A.;Mori,I.;Horinouchi,A.Toxicol.Mech.Methods 2009,19(8),477–485.
Natalie,M.;Margino,S.;Erik,H.;Annelieke,P.;Geert,V.;Philippe,V.Toxicol.in Vitro 2009,23(2),217–226.
Sawada,H.;Taniguchi,K.;Takami,K.Toxicol.in Vitro 2006,20
(8),1506–1513.
Vitovic,P.;Alakoskela,J.M.;Kinnunen,P.K.J.J.Med.Chem.
2008,51(6),1842–1848.
De Vendittis,E.;Palumbo,G.;Parlato,G.;Bocchini,V.Anal.Biochem.1981,115,278–286.
Deb,N.;Shannigrahi,M.;Bagchi,S.J.Phys.Chem.B 2008,112
2868–2873.
Moyano,F.;Silber,J.J.;Correa,N.M.J.Colloid Interface Sci.
2008,317,332–345.
Moyano,F.;Biasutti,M.A.;Silber,J.J.;Correa,N.M.J.Phys.Chem.B 2006,110,11838–11846.
Gum,R.J.;Hickman,D.;Fagerland,J.A.;Heindel,M.A.;Gagne,G.D.;Schmidt,J.M.;Michaelides,M.R.;Davidsen,S.K.;Ulrich,R.G.Biochem.Pharmacol.2001,62(12),1661–1673.
Wilson,B.D.;Clarkson,C.E.;Lippmann,M.N.Am.Rev.Respir.Dis.1991,143,1110–1114.
Lahoti,S.;Lee,W.M.Gastroenterol.Clin.North Am.1995,24
(4),907–922.
Kita,N.;Sugihara,N.;Furuno,K.J.Pharmacobiodyn.1992,15
(4),181–189.
Giuliano,R.A.;Paulus,G.J.;Verpooten,G.A.;Pattijn,V.M.;Pollet,D.E.;Nouwen,E.J.;Carlier,M.B.;Maldague,P.;Tulkens,P.M.;Debroe,M.E.Hum.Toxicol.1984,3(5),432.
Kacew,S.;Narbaitz,R.;Ruddick,J.A.;Villeneuve,D.C.Exp.Mol.Pathol.1981,35(1),98–107.
Kodavanti,U.P.;Mehendale,H.M.Am.J.Respir.Cell Mol.Biol.
1991,4(4),369–378.
Antonini,J.M.;Reasor,M.J.Biochem.Pharmacol.1991,42
S151–S156.
Kannan,R.;Sarma,J.S.M.;Guha,M.;Venkataraman,K.Eur.J.Pharmacol.1990,183(6),2452–2453.
Nattel,S.J.Cardiovasc.Pharmacol.1986,8(4),771–777.
Latini,R.;Tognoni,G.;Kates,R.E.Clin.Pharmacokinet.1984,9(2),136–156.
Riley,R.J.;Roberts,P.;Kitteringham,N.R.;Park,B.K.
Biochem.Pharmacol.1990,39(12),1951–1958.
Lambert,C.;Park,B.K.;Kitteringham,N.R.Biochem.Pharmacol.1989,38(17),2853–2858.
Wojcikowski,J.;Boksa,J.;Daniel,W.A.Biochem.Pharmacol.
2010,80(8),1252–1259.
Stevens,J.C.;Shipley,L.A.;Cashman,J.R.;Vandenbranden,M.;Wrighton,S.A.Drug Metab.Dispos.1993,21(5),753–760.
Hartmann,F.;Gruenke,L.D.;Craig,J.C.;Bissell,D.M.Drug Metab.Dispos.1983,11(3),244–248.
Gupta,R.N.;Molnar,G.;Hill,R.E.;Gupta,M.L.Clin.Biochem.1976,9(5),247–251.
Prox,R.;Breyer-Pfa?,U.Drug Metab.Dispos.1987,15(6),890–896.
Vandemark,F.L.;Adams,R.F.;Schmidt,G.J.Clin.Chem.
1978,24(1),87–91.
Kim,K.A.;Park,J.Y.;Lee,J.S.;Lim,S.Arch.Pharm.Res.2003,26(8),631–637.
Projean,D.;Baune,B.;Farinotti,R.;Flinois,J.P.;Beaune,P.;Taburet,A.M.;Ducharme,J.Drug Metab.Dispos.2003,31(6),748–754.
Wu,Z.L.;Huang,S.L.;Ou-Yang,D.S.;Xu,Z.H.;Xie,H.G.;Zhou,H.H.Zhongguo Yao Li Xue Bao 1998,19(5),433–436.
Nielsen,K.K.;Flinois,J.P.;Beaune,P.;Brosen,K.J.Pharmacol.Exp.Ther.1996,277(3),1659–1664.
Max?eld,F.;McGraw,T.Nat.Rev.Mol.Cell Biol.2004,5
121–132.
Sawada,H.;Takami,K.;Asahi,S.Toxicol.Sci.2005,83(2),282–292.
Toubeau,G.;Nonclercq,D.;Zanen,J.;Lambricht,P.;Tulkens,
P.M.;Heuson Stiennon,J.A.;Laurent,G.Kidney Int.1991,40(4),691–699.
Poucell,S.;Valencia,P.;Ireton,J.;Downar,E.;Patterson,J.;Blendis,L.;Phillips,M.J.Hepatology 1983,3(5),805.
Poucell,S.;Ireton,J.;Valenciamayoral,P.;Downar,E.;Larratt,L.;Patterson,J.;Blendis,L.;Phillips,M.J.Gastroenterology 1984,86(5),926–936.
Goldman,I.S.;Winkler,M.L.;Raper,S.E.;Barker,M.E.;Keung,E.;Goldberg,H.I.;Boyer,T.D.Am.J.Roentgenol.1985,144(3),541–546.
Riva,E.;Marchi,S.;Pesenti,A.;Bizzi,A.;Cini,M.;Veneroni,E.;Tavbani,E.;Boeri,R.;Bertani,T.;Latini,R.Biochem.Pharmacol.1987,36(19),3209–3214.
Hruban,Z.Environ.Health Perspect.1984,55,53–76.
Kodavanti,U.P.;Lockard,V.G.;Mehendale,H.M.J.Biochem.Toxicol.1990,5(4),245–251.
Lullmann-Rauch,R.;Nassberger,L.Acta Pharmacol.Toxicol.
1983,52,161–167.
Yano,T.;Ohmori,S.;Igarashi,T.;Ueno,K.;Kitagawa,H.Jpn.J.Pharmacol.1987,43,207.
Gray,J.E.;Weaver,R.N.;Stern,K.F.;Phillips,W.A.Toxicol.Appl.Pharmacol.1978,45(3),701–711.
Lullmann-Rauch,R.;Reil,G.H.Arch.Pharmacol.1974,
285,175–184.
(68)Valodia,P.N.;Syce,J.A.Med.Sci.Res.1998,26(7),491–493.
Gonzalezrothi,R.J.;Zander,D.S.;Ros,P.R.Chest 1995,107
(6),1763–1765.
Auberttulkens,G.;Vanhoof,F.Arch.Int.Physiol.Biochim.Biophys.1978,86(2),403–405.
Pakuts,A.P.;Parks,R.J.;Paul,C.J.;Bujaki,S.J.;Mueller,R.W.
Res.Commun.Chem.Pathol.Pharmacol.1990,67(1),55–62.
Staubli,W.;Schweizer,W.;Suter,J.Exp.Mol.Pathol.1978,
28,177–195.
Glaumann,H.;Bronner,U.;Ericsson,O.;Gusta?son,L.L.;Rombo,L.Pharmacol.Toxicol.1994,74,17–22.
Lullmann,H.;Lullmann-Rauch,R.Klin.Wochenschr.1978,
56,309–310.
Kasahara,T.;Tomita,K.;Murano,H.;Harada,T.;Tsubakimoto,K.;Ogihara,T.;Ohnishi,S.;Kakinuma,C.Toxicol.Sci.2006,90(1),133–141.
Beresford,A.P.;McGibney,D.;Humphrey,M.J.;Macrae,P.V.;Stopher,D.A.Xenobiotica 1988,18(2),245–254.
Stopher,D.A.;Beresford,A.P.;Macrae,P.V.;Humphrey,M.J.
J.Cardiovasc.Pharmacol.1988,12,S55–S59.
Pirmohamed,M.;Williams,D.;Madden,S.;Templeton,E.;Park,B.K.J.Pharmacol.Exp.Ther.1995,272(3),984–990.
Tugnait,M.;Hawes,E.M.;McKay,G.;Eichelbaum,M.;Midha,K.K.Chem.Biol.Interact.1999,118(2),171–189.
Delta-8使用新方法測試CMC,而不是表面張力測試法——摘要
Delta-8使用新方法測試CMC,而不是表面張力測試法——方法










