合作客戶/
拜耳公司 |
同濟大學 |
聯合大學 |
美國保潔 |
美國強生 |
瑞士羅氏 |
相關新聞Info
推薦新聞Info
-
> 定性分析聚合物界面張力與系統黏度比之間的關系——數值仿真結果、結論
> 定性分析聚合物界面張力與系統黏度比之間的關系——數值模擬、實驗研究結果
> 定性分析聚合物界面張力與系統黏度比之間的關系——實驗部分
> 探究LB復合膜的酸致變色特性
> 受磷脂雙分子層啟發構建ZIBs兩性LB膜——制備高性能碘正極新思路
> 納米活性顆粒表面潤濕性測量方法及具體操作步驟
> 人工沖洗升級為超聲波清洗,可改善新能源電池沖壓配件的表面張力
> LB法組裝Silicalite-1型分子篩晶粒層,制備出高度b-軸取向的ZSM-5分子篩膜
> 微量天平高靈敏測定雞肉中磺胺類藥物含量
> 超低軌衛星環境效應研究也會用到超微量天平?
電極與溶液界面的吸附現象
來源:電化學學習 瀏覽 1871 次 發布時間:2022-04-12
我們知道了物理吸附和化學吸附,那么在電極溶液界面上同樣也會發生吸附現象。
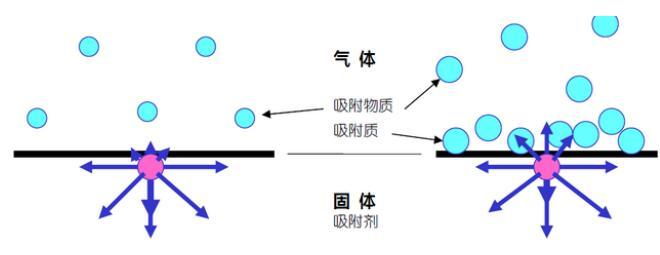
但是因為界面上存在著電場作用,所以說其吸附現象除了原有吸附的規律以外,還有著一些特殊的規律。
比如之前所說在電極表面帶有剩余電荷的時候,會在靜電作用下使具有相反電荷的離子聚集到界面區,這種吸附稱為靜電吸附。其次還有非靜電力作用的特性吸附。

我們這邊定義能在電極溶液界面發生吸附的物質稱為表面活性物質,它可以使界面張力(液體與另一種不相混溶的液體接觸,其界面產生的力叫液相與液相間的界面張力)降低。
我們知道在溶液中電極表面是吸附了一層極性水分子的。就是緊密層第一層定向排列的水分子偶極層。所謂的表面活性物質只有脫去其外部的水化膜,并且擠掉吸附在電極表面的水分子,才有可能與電極表面發生短程作用而聚集在界面,也就是成為表面活性物質。比如在前面說緊密層結構時候的陰離子。
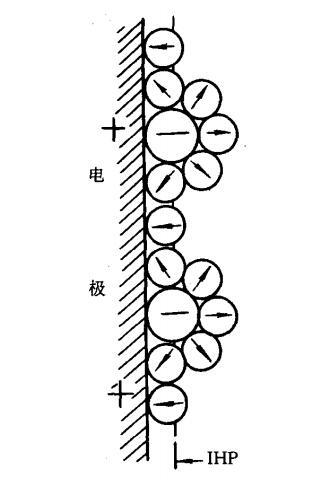
表面活性物質與電極表面發生的短程相互作用,包括鏡像力,色散力和類似于化學鍵的化學作用。
表面活性粒子脫水化和取代水分子的過程將使體系自由能增加。與之相對應的短程相互作用將使體系自由能減少。這兩者相互抵消,如果可以使體系總的自由能減少就可以使吸附過程發生。
所以不同的物質發生特性吸附的能力不同,同一物質在不同電極體系中的吸附行為也不相同。本質的原因就在于體系自由能的變化并不相同。
自由能的定義是指在一個熱力過程中,系統減少的內能中可以轉變為對外做功的那部分,所謂對外做功的那部分實際上就是指有用的能量。
可以將其分為亥姆霍茲定容自由能和吉布斯定壓自由能。吸附過程使自由能降低,實際上無非就是指這樣一個吸附過程,是消耗有用功的。

電極溶液界面吸附現象對電極過程動力學有重大影響。即使表面活性粒子不參與電極反應,他們的吸附也會改變電極表面狀態和雙電層中電位分布。
從而必然會影響反應粒子在電極表面的濃度和電極反應的活化能(分子從常態轉變為容易發生化學反應的活躍狀態所需要的能量,催化劑的作用就在于改變反應所經過的途徑,從而改變反應的活化能),使電極反應速度發生變化。
而如果表面活性粒子是反應粒子或反應產物的時候,就會直接影響到相關步驟的動力學規律。










